马上注册,结交更多好友,享用更多功能,让你轻松玩转社区。
您需要 登录 才可以下载或查看,没有账号?立即注册

x
作者:淼淼 + f' a, [& D: i6 E& \! Q0 L. K0 H
三阴性乳腺癌(TNBC)作为乳腺癌的其中一种亚型,约占总体乳腺癌人群的10-20%,其雌激素受体(ER)、孕激素受体(PR)以及人表皮生长因子受体2(HER2)表达均为阴性。 - b* ` F/ [, j( e9 o& z
这类乳腺癌恶性程度高,容易出现内脏转移,复发风险大,预后较差,且既往缺乏有效的专项治疗策略,素有最“毒”乳腺癌之称。
4 ^. z3 r" b3 K/ o7 D近年来,有不少研究显示,免疫治疗尤其是免疫联合其他疗法已在TNBC中取得突破。 * d( x, J2 Z6 V1 c. j* ^6 z3 i$ {
III期IMpassion130研究显示,阿替利珠单抗+白蛋白紫杉醇可延长转移性TNBC患者ITT(意向性分析)人群和PD-L1阳性患者的无进展生存期(PFS)。 8 z( I' `! ~- V' F5 }$ D& ]
在PD-L1阳性患者中,联合组和安慰剂+白蛋白紫杉醇组的中位PFS分别为7.5个月和5.0个月,两组的mOS(中位总生存期)分别为25.4个月和17.9个月。KEYNOTE-355研究显示,帕博利珠单抗+化疗(9.7个月)对比安慰剂+化疗(5.6个月)可显著改善PD-L1 CPS≥10患者的PFS。 ) v2 {$ h* _- r
2 W: T, F! q1 }8 w$ a- ]' ]! K( y
但是,并不是所有PD-L1阳性的TNBC患者都可从免疫治疗中获益。鉴别出能从免疫治疗中获益的患者特征是实现精准治疗的主要需求;更精确地区分患者分子分型和开发更有效的联合方案也是亟需解决的问题。 ) d2 Y% M, I1 C1 a6 v) ^
早在2011年,Lehmann等通过基因表达谱特征初步绘制了TNBC分子亚型图谱,但是这种分型的方法学过于单一,特别是无法反映肿瘤的基因组学特征。 5 _/ F$ m3 f7 y1 g- Y' T/ X! i3 Q m
2012年癌症基因组图谱(TCGA)工作组通过6种不同的技术平台评估了100多例三阴性乳腺癌样本的肿瘤分子特征,但关于分型指导的诊疗实践却相对缺乏,因此也无法在临床中更广泛的应用。 & ^+ M# a# ?* ?0 W
而在2019年,复旦大学附属肿瘤医院邵志敏教授团队绘制出全球最大的三阴性乳腺癌多组学图谱并提出“复旦分型”标准,证实三阴性乳癌并不是一种单一类型的疾病,其实是个鱼龙混杂的集体,深入研究有望对这个集体进一步细分类型。团队提出通过基因序列和表达加强研究,或将破解三阴性乳腺癌“无靶点”的难题,为寻找到三阴性乳腺癌的靶点指明新的方向。 ) X0 ^- i/ h& a8 U# F5 O. M4 `
研究团队于2019年发表在《Cancer Cell》的文章首次阐明了中国人群TNBC的分子特征,并细化了TNBC的分子分型。
# o) S1 o% O: {) ~1 b$ J通过全外显子组测序(WES)、拷贝数变异(CNA)分析和RNA测序等多组学技术对465例连续的TNBC患者样本进行分析,最终将TNBC分成四个亚型,分别为:管腔雄激素受体型(LAR,占比23%)免疫调节型(IM,占比24%)、基底样免疫抑制型(BLIS,占比39%)和间充质型(MES,占比15%),这种分型结果与Lehmann等发布的研究结果具有相关性。
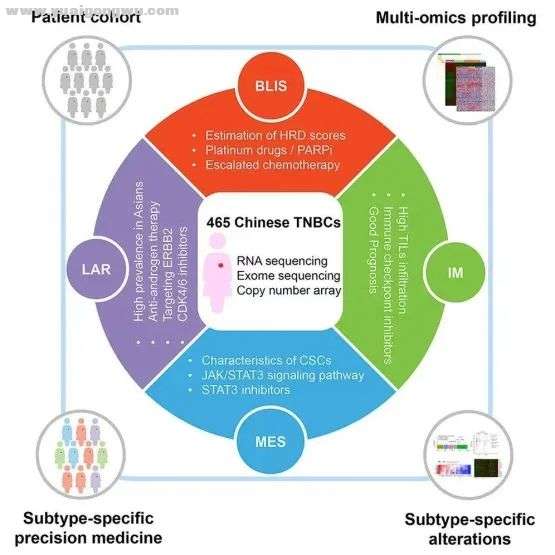
“复旦分型”详情
% z7 m% Z7 T" \8 W- q研究表示,四种分型的预后和分子特征具有一定的差异。
7 b: O: m$ r0 s$ L$ C
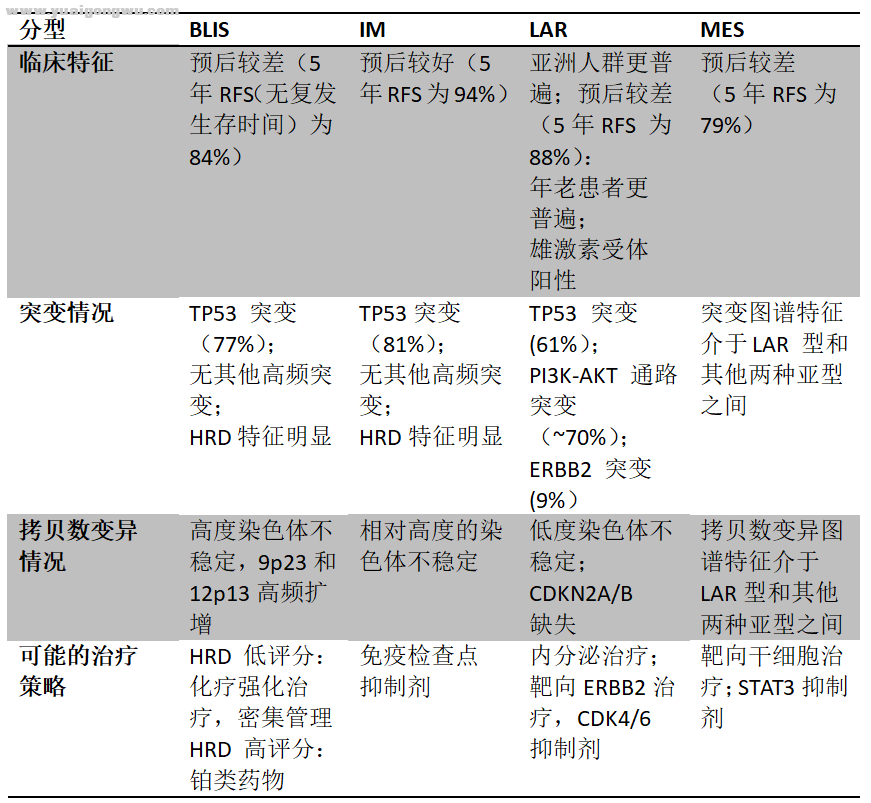 : C9 E3 {3 Y3 m. H! j
: C9 E3 {3 Y3 m. H! j
而在团队进一步的FUTURE研究中,基于“复旦分型”采用不同方案治疗多线耐药的mTNBC(转移性三阴性乳腺癌)患者,研究人员发现IM型(CD8免疫组化染色≥10%)患者对免疫治疗应答良好。 # C! B' e L" h7 x
在之前的动物实验证实,抗血管生成小分子药物法米替尼(famitinib)不仅可以增加CD8+ T细胞的浸润能力还能增强程序性死亡受体-配体 1(PD-L1)的表达,该药物联合免疫治疗和化疗可以更有效地抑制三阴性乳腺癌生长。
) y' c9 g/ T+ U6 M |/ p9 R基于前期研究发现,研究团队将FUTURE-C臂的方案推进至一线治疗,开展了名为FUTURE-C-Plus的临床试验。FUTURE-C-PLUS试验是一项开放标签、单臂、II期临床试验,纳入条件为既往未接受过系统治疗的无法切除、局部晚期或转移性IM型TNBC患者。旨在评估法米替尼+卡瑞利珠单抗+白蛋白紫杉醇在CD8阳性晚期TNBC患者中的疗效。
& K$ \ L @5 u& T, g' t5 B在2019年10月至2020年10月,该研究筛选了122例患者,其中48例免疫组化染色CD8阳性患者入选并接受治疗,所有患者均纳入意向性分析(ITT)和安全性分析人群,其中46名患者属遵循研究方案的治疗(PP)人群;入组患者的中位年龄为50岁。 4 `8 h% ]! {5 a/ C* J+ B6 l
符合条件患者在第1-28天接受法米替尼(20mg 口服)治疗,在第 1 天和第 15 天接受卡瑞利珠单抗治疗(200 mg,静脉注射),在每周期的第1、8、15天接受白蛋白紫杉醇(100mg/m2)治疗,4周为一周期。主要研究终点为研究者评估的客观缓解率(ORR),次要终点为PFS和总生存期(OS),缓解持续时间(DOR)和安全性。 6 D$ a- O8 F- d
研究人员表示,截至2021年10月12日,中位随访时间为17.0个月,18名(37.5%)患者仍在接受治疗;23名(47.9%)患者转移部位超过3处,肺转移24例(50.0%),肝转移10例(20.8%)。

入组患者流程
5 M/ r' M6 ~; b. c& d" s: g从研究数据来看,ITT(意向性分析)人群中,44例(95.7%)患者出现了靶病灶缩小。39例(81.3%)患者达到确认的客观缓解,其中5例患者达到完全缓解(CR),34例患者达到部分缓解(PR),中位至缓解时间为1.9个月。 9 o! e! d* R+ U+ N: D+ d, Q
在39例缓解者中,中位DOR为14.9个月,其中18例缓解者考虑还在缓解,DCR(疾病控制率)为95.8%。另外,25例(52.1%)患者疾病进展,16例(33.8%)患者死亡,中位PFS为13.6个月。中位OS未达到,12个月OS率和18个月OS率分别为82.6%和54.4%。
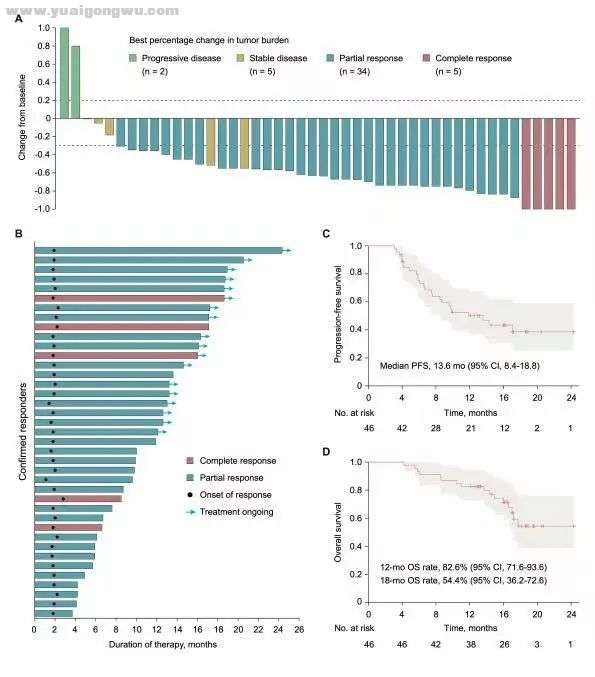
患者治疗响应情况和疗效指标
: U, C* S0 L4 ?4 X1 R* T就安全性而言,三药联合治疗的耐受性良好,仅有两名患者因不良事件而停止治疗;最常见的3级或4级治疗相关不良事件(TRAEs)是中性粒细胞减少症(33%),并且这一不良反应通过剂量调整和粒细胞集落刺激因子的使用,也是可控和可逆的。 * v: o7 {9 O6 ]& p* O
但值得注意的是,有54.2%(26/48)患者发现促甲状腺激素(TSH)升高,这可能是因为法米替尼和卡瑞利珠单抗的联合使用;20%的患者出现了不同程度的甲状腺功能减退,但只有2例(4.2%)为3级;19例患者(39.6%)发生了法米替尼相关的不良事件,其中3级不良事件主要为高血压(2例)和蛋白尿(1例)。 + Y- h) d6 c& j( S2 k3 ]+ D0 j
所有患者都接受了至少一个完整的治疗周期,白蛋白紫杉醇的中位治疗周期为8个,卡瑞利珠单抗和法米替尼的中位治疗周期为10个;治疗过程中大多数患者法米替尼剂量从20mg减至15mg,较低剂量的法米替尼是否会导致更持久的反应目前尚不清楚,这个组合的最佳剂量和用药时间,还需要更多的临床试验去验证。
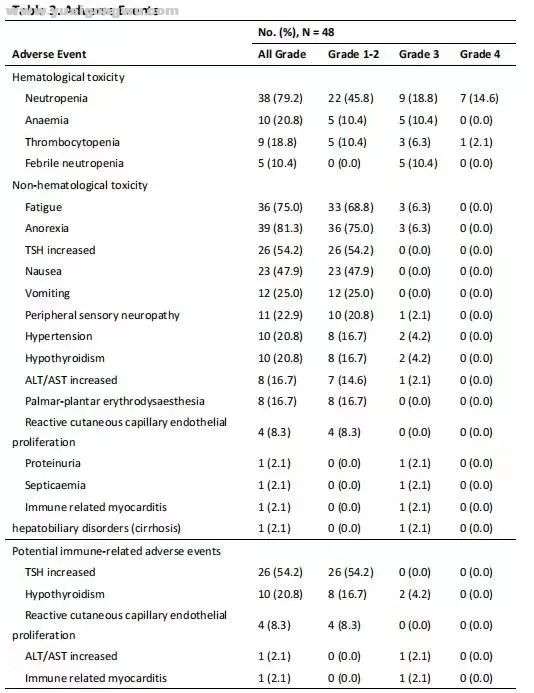
不良反应
! X8 o2 k" U2 ?. [8 @+ ]$ b9 h8 l就生物标志物而言,晚期IM型TNBC患者中最常见的基因突变为TP53(78%)、BCOR(13%)、BRCA1(13%)、KAT6A(13%)和RRM2(13%)。研究者分析了常见体细胞突变和肿瘤缓解情况的相关性。总体上,KAT6A与客观缓解呈正相关(P=0.044),而BRCA1(P = 0.055)和PKD1(P = 0.034)与客观缓解呈负相关。 * u: v6 _6 N) [9 D
此外,老年患者从治疗中获益更多,3个转移灶以上患者的疗效较差。骨转移提示从治疗中获益更少。PD-L1不能预测疗效,但PD-L1联合CD31具有预测价值,总体上,PD-L1和CD31阴性患者对联合治疗的应答较差。 ' A2 y5 C6 c( \8 p. \* M# D5 j
研究者还发现间质浸润淋巴细胞(sTIL)与CD8呈正相关性,因此,采用sTIL 识别免疫调节型 TNBC 亚型可能是未来研究方向之一。

治疗应答相关基因组分析和生物标志物分析
9 a- t& D0 b2 s1 q总的来说,在这个研究中,法米替尼、卡瑞利珠单抗和白蛋白紫杉醇的新组合作为无法切除、局部晚期或转移性IM型TNBC患者的一线治疗,显示出显著的抗肿瘤活性和可控的毒性,三药联合方案有望作为晚期IM型TNBC患者潜在一线治疗选择;研究中发现的治疗反应预测标志物,也为IM型TNBC患者临床结局的预测和治疗方案的选择提供了新的思路。 9 N- Y D$ x( r- K- H5 }3 W+ a
我们期待“三阴性乳腺癌复旦分型”的研究结果能够逐渐的在临床中继续得到推广和应用,并期待其后续更多研究数据的发布。
! B% i A6 d1 m) O |